El Dr. Maravillas Montero es Químico Bacteriólogo y Parasitólogo por la Escuela Nacional de Ciencias Biológicas del IPN, con una Maestría y Doctorado en Biomedicina Molecular por el CINVESTAV del IPN. Realizó una estancia posdoctoral en la Universidad de California, Irvine, en Estados Unidos. Es investigador titular en el Instituto de Biotecnología de la UNAM, con área de especialidad en la inmunología celular y molecular. Recibió en 2021 el Premio Nacional de Inmunología para Investigadores Jóvenes. Es integrante del Sistema Nacional de Investigadoras e Investigadores y miembro de la Academia de Ciencias de Morelos.
Esta publicación fue revisada por el comité editorial de la Academia de Ciencias de Morelos.
Acercando la complejidad a un nivel individual
Imaginemos una fábrica, donde se produce algún producto cualquiera. Dentro de esa fábrica trabaja mucha gente: desde el personal de intendencia, los obreros, el personal de administración, los ingenieros, los altos ejecutivos y muchos más. Cada individuo afiliado a alguna oficina o sitio de trabajo particular dentro de la compañía, desempeña funciones específicas para que todo el sistema funcione adecuadamente y en armonía; o al menos eso sería lo ideal. Hay compañías que funcionan durante años sin mayores problemas; mientras cada parte cumpla su papel, en realidad nadie se cuestiona cómo opera todo el conjunto. Pero cuando algo se rompe, cuando una oficina deja de hacer su trabajo, cuando alguna persona o grupo actúa autoritariamente, cuando ciertos trámites se multiplican sin razón, o simplemente cuando deja de haber agua en los baños, los trabajadores de la empresa pueden notar que algo está mal y que necesita corregirse. Visto desde fuera, alguien podría decir que esa compañía no funciona; sin embargo, los trabajadores de la empresa podrán fácilmente identificar a algunos de sus compañeros como responsables de esos fallos. Entonces, es sencillo entender que no se trata de la empresa en general, sino de acciones y omisiones concretas, efectuadas por actores específicos.
Durante décadas, la biomedicina ha estudiado al cuerpo humano con una visión muy parecida. Hemos aprendido a describir las enfermedades, sean cuales sean, a partir de promedios: qué genes aumentan su actividad, produciendo más RNA mensajeros y por ende más de una proteína específica, qué moléculas se elevan en la sangre o qué señales predominan en un tejido dañado. No malinterpretemos, esta información ha sido crucial para el desarrollo de diagnósticos y tratamientos eficaces. Sin embargo, como ocurre con cualquier generalización, esto tiene limitaciones claras: si bien podemos entender cómo funciona alguna parte de nuestro cuerpo (algún órgano o tejido), este enfoque basado en promedios no nos permite entender el papel de las células individuales que lo componen. Regresando a nuestro ejemplo de una compañía, sería como decir que todos los trabajadores hacen más o menos lo mismo, cuando podemos detectar que cada uno tiene funciones específicas.
Este límite se vuelve especialmente evidente en dos grandes grupos de enfermedades, donde los problemas los inician los propios “trabajadores” de la “fábrica”: las enfermedades autoinmunes y el cáncer. En las enfermedades autoinmunes, el sistema inmunológico, que normalmente nos protege de infecciones, se confunde y ataca por error a las propias células y tejidos del cuerpo, causando inflamación y daño grave. Por otro lado, el cáncer se produce cuando algunas células pierden el control sobre su crecimiento y comienzan a multiplicarse desordenadamente, formando tumores o invadiendo otros tejidos.
Estudiando las enfermedades modernas más temidas con visión individualizada
Tanto en el cáncer como en las enfermedades autoinmunes, el problema rara vez es uniforme. No es que todas las células del sistema inmunológico se comporten mal, ni que todas las células tumorales sean idénticas. Por el contrario, casi siempre son poblaciones celulares específicas en estados muy particulares las que desencadenan el daño, mantienen la inflamación o se resisten a los tratamientos. Cuando todo se analiza en conjunto, esas pequeñas diferencias dadas por esas poblaciones celulares, no se aprecian con facilidad.
En los últimos años, una nueva tecnología ha empezado a cambiar esta forma de mirar: la secuenciación de RNA de célula única (single-cell RNA sequencing o simplemente scRNA-seq). Esta tecnología permite evaluar todo el conjunto de RNAs mensajeros (esto es, qué genes están activos) dentro de células individuales en un tejido: no produce un solo reporte global del estado de un tejido, sino que arroja una biblioteca completa de datos provenientes de cada célula individual. Hace algo más parecido a hacer una auditoría en la fábrica, revisando uno por uno los informes de trabajo que reporta cada trabajador. Cada célula analizada así queda registrada como una unidad funcional independiente, con lo que podemos apreciar por ejemplo qué genes estaba utilizando en ese momento específico, qué programas biológicos tenía activos o cómo respondía a su entorno inmediato.
La secuenciación de célula única, tecnología novedosa y poderosa
Técnicamente, la secuenciación de RNA de célula única inicia con la extracción y purificación de las frágiles moléculas de RNA (ácido ribonucleico) mensajero de células individuales en un conjunto o mezcla celular. Estas moléculas se producen de forma natural y permiten que los genes se expresen y cumplan con funciones específicas, que le dan identidad a cada célula en nuestro organismo. Estos RNAs se convierten posteriormente en un tipo de molécula más estable llamado cDNA (ácido desoxirribonucleico complementario) que puede manipularse con mayor facilidad para ser secuenciado o leído en equipos especializados. Este modo de secuenciación arroja una cantidad tremenda de datos, que son analizados con ayuda de programas computacionales complejos que permiten llegar a conclusiones sobre el estado individual de cada célula analizada (Figura 1).
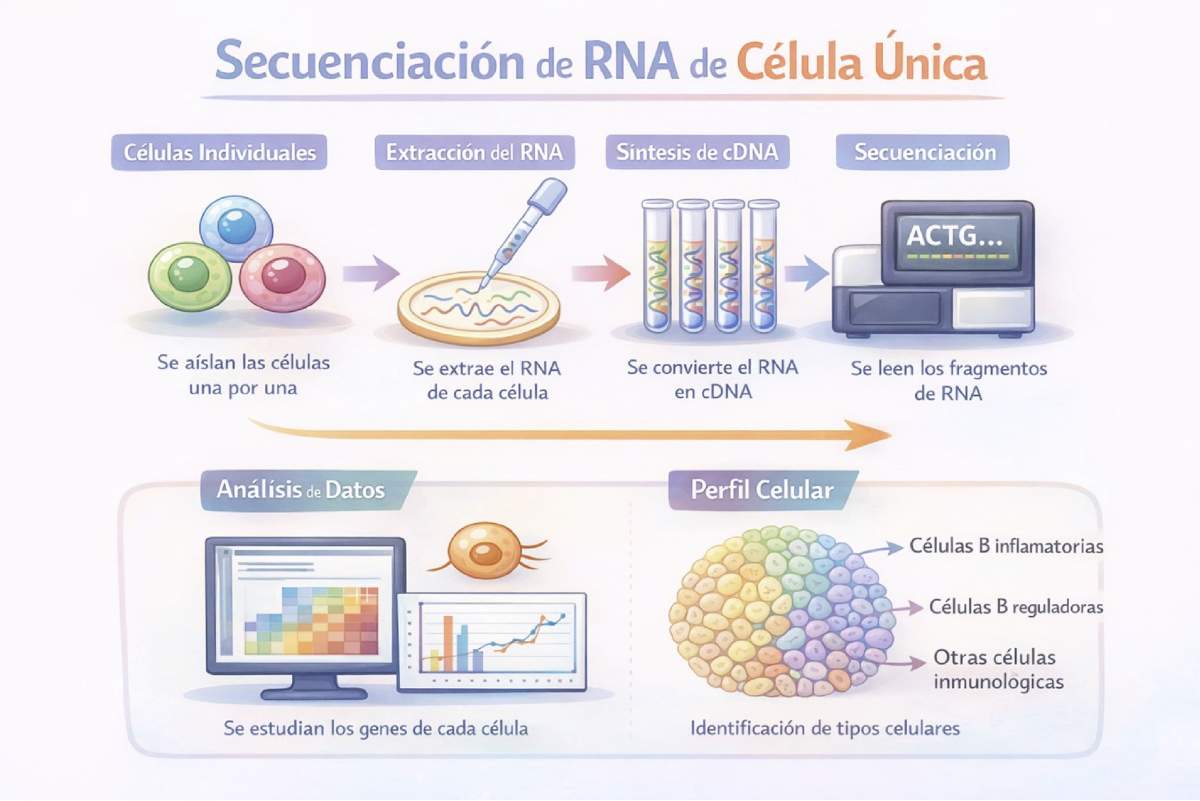
Figura 1. Proceso simplificado de la secuenciación de RNA de célula única. Primero se aíslan células individuales, luego se extrae su RNA y se convierte en DNA complementario (cDNA) para poder leer su secuencia. Finalmente, mediante análisis computacionales, se comparan los perfiles de expresión génica y se identifican los distintos tipos celulares presentes en una muestra. Creado por el autor con Gemini (Google).
Este cambio de la escala respecto a cómo analizamos las muestras o biopsias de algún paciente, ha revelado una realidad tan incómoda como fascinante: incluso células que parecen idénticas dentro de un mismo órgano o tejido pueden estar desempeñando funciones radicalmente distintas, e incluso opuestas. Algunas activan respuestas inflamatorias, otras las apagan; algunas cooperan con el sistema inmunológico, mientras que otras aprenden a evadirlo. En ese mosaico de comportamientos se define el curso de los padecimientos a los que nos referimos aquí.
En las enfermedades autoinmunes, esta mirada ha permitido entender que el sistema inmune no actúa como un bloque homogéneo que de pronto “se equivoca”, sino como una red compleja en la que ciertos circuitos se sobreactivan y otros dejan de funcionar. En pacientes con lupus, artritis reumatoide o esclerosis múltiple, por ejemplo, se han identificado poblaciones de células inmunológicas con programas inflamatorios bien definidos, que están ausentes o son poco frecuentes en personas sanas. Inclusive, dos pacientes con el mismo diagnóstico clínico pueden en realidad, tener problemas celulares distintos, lo que ayuda a explicar por qué responden de manera diferente al mismo tratamiento médico.
Las células B (un componente importante del sistema inmune) ofrecen un ejemplo muy ilustrativo. Durante mucho tiempo se les entendió casi exclusivamente como fábricas de anticuerpos que podían neutralizar microorganismos o toxinas. Hoy sabemos que cumplen funciones mucho más diversas. Curiosamente, en varias enfermedades autoinmunes, los tratamientos más comunes incluyen aquellos que tratan de erradicar a este tipo celular del organismo; tratamientos que en muchos pacientes funcionan pero en otros no. La secuenciación de célula única ha permitido distinguir poblaciones de células B que participan activamente en la inflamación dañina, de otras que desarrollan funciones protectoras (células reguladoras). Este hallazgo refuerza una idea clave para la medicina contemporánea: no siempre es necesario eliminar poblaciones completas de células, sino intervenir sobre subpoblaciones de las mismas que resultan dañinas.
En el cáncer, el impacto de esta tecnología ha sido igualmente profundo. Un tumor ya no se concibe como una masa uniforme, sino como un ecosistema celular dinámico (Figura 2). Dentro de un tumor, algunas células se reproducen de forma agresiva, otras entran en estados de reposo, otras modifican su entorno para evitar ser atacadas por el sistema inmune. Si bien todas estas células cooperan entre sí para producir un tumor agresivo, su número, tipo y disposición en el tumor puede variar, aún entre tumores que parecían pertenecer al mismo tipo. La secuenciación de célula única ha permitido mapear estas diferencias individuales y entender por qué ciertos tratamientos oncológicos funcionan sólo en algunos pacientes, mientras que en otros resultan lamentablemente inútiles.
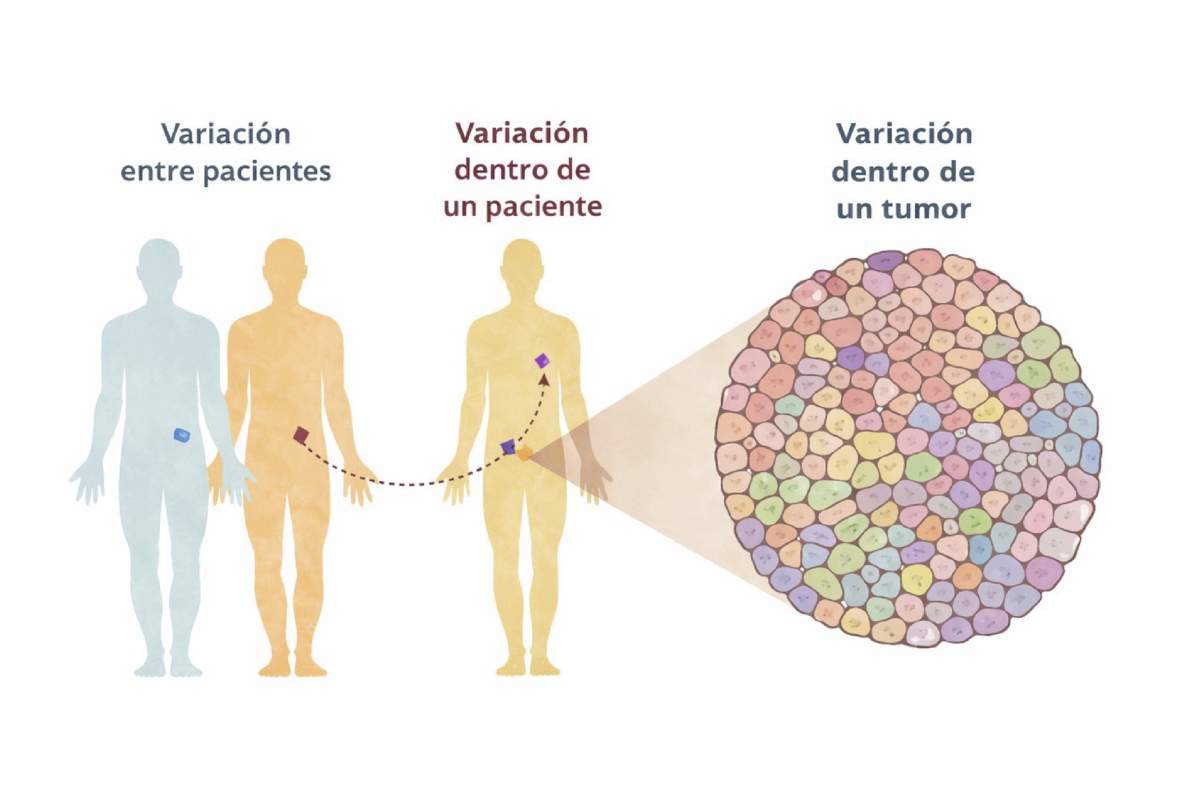
Figura 2. La secuenciación de RNA de célula única permite estudiar la actividad de los genes en distintos niveles. Mientras que la secuenciación masiva convencional ofrece un promedio de la expresión génica entre diferentes pacientes o dentro de una muestra completa, la secuenciación de RNA de célula única revela las diferencias entre las células individuales, haciendo visible la diversidad celular que existe dentro de un mismo tumor o tejido y que pueden apreciarse en la imagen de distintos colores. Adaptado de Fox y Loeb, 2014.
La secuenciación de célula única y su impacto en la medicina
El desarrollo de esta técnica es particularmente relevante en el campo de la inmunoterapia, que involucra intervenciones que manipulan la funcionalidad del sistema inmune de un paciente, para hacerlo más eficiente en el control o erradicación de estas enfermedades. A pesar de ser lo más lógico, la simple presencia de células inmunes en un tumor no garantiza una respuesta favorable: lo que importa en realidad es qué tipo de células están presentes ahí y en qué estado se encuentran. Algunas están listas para atacar; otras están agotadas; otras más contribuyen a suprimir la respuesta inmune. Estas diferencias, invisibles en los análisis tradicionales, se vuelven evidentes cuando se observa célula por célula.
Otro aporte crucial ha sido la comprensión de la resistencia a los tratamientos. En muchos casos, las células resistentes ya existen antes de iniciar la terapia, aunque sean pocas. El tratamiento elimina a las células sensibles y deja espacio para que esas subpoblaciones se expandan. Desde esta perspectiva, la resistencia no es un accidente, sino un proceso de selección a veces acelerado por las mismas terapias que se emplean equivocadamente. Identificar estas células a tiempo podría permitir estrategias terapéuticas personalizadas y más efectivas. El conocer estas diferencias permitiría conocer de manera individual a la enfermedad que se desea erradicar y conociendo sus fortalezas y debilidades, diseñar una terapia que sea efectiva para cada paciente.
A pesar de su enorme potencial, la secuenciación de célula única aún enfrenta retos importantes para su uso rutinario en la clínica. Es una tecnología bastante costosa, técnicamente compleja y que genera grandes volúmenes de datos que no son sencillos de analizar. Por ello, su impacto inmediato probablemente no será a manera de una prueba diagnóstica universal, sino como fuente de conocimiento para identificar marcadores de enfermedad más simples y fácilmente determinables. Muchos de los avances actuales consisten en traducir lo aprendido con scRNA-seq a pruebas que puedan realizarse con técnicas convencionales, más baratas y accesibles. Sin embargo, podemos anticipar que no se quedarán solo en eso. Cualquier tecnología innovadora en un principio es cara, compleja y difícil de aplicar. Pero son precisamente las ventajas que ofrecen las que actúan como alicientes para encontrar maneras de abaratarlas, volverlas simples en su aplicación y convertirlas en entendibles para quienes tengan que usarlas.
De esta manera, la tecnología de secuenciación de RNA de célula única ofrece una lección clara: comprender un sistema complejo no consiste sólo en medirlo en conjunto, sino en reconocer quién toma las decisiones dentro de él. Y contrario a lo que podría pensarse al desmenuzar la integridad de las muestras de tejidos, “leer” la biología célula por célula no deshumaniza la medicina; al contrario, la acerca a la singularidad de cada paciente.
Tal vez el mayor aporte de la secuenciación de célula única no sea técnico, sino conceptual. Nos recuerda que los grandes problemas, en las organizaciones y en los organismos, rara vez se originan en todas partes al mismo tiempo. Suelen comenzar en lugares específicos, con protagonistas concretos. Aprender a identificarlos es hoy, una de las fronteras más prometedoras de la medicina contemporánea… la llamada y tan anhelada medicina de precisión.
Para saber más
- Boxer E et al. (2025). Emerging clinical applications of single-cell RNA sequencing in oncology. Nature Reviews Clinical Oncology 22:315-326.
https://doi.org/10.1038/s41571-025-01003-3
- Fox EJ, Loeb LA. (2014). Cancer: One cell at a time. Nature 512(7513):143-144. doi: 10.1038/nature13650.
- Huang J et al. (2025). Single-cell RNA sequencing in autoimmune diseases: New insights and challenges. Pharmacol Ther 267:108807. doi: 10.1016/j.pharmthera.2025.108807.
- Lähnemann D et al. (2020). Eleven grand challenges in single-cell data science. Genome Biology 21:31. https://doi.org/10.1186/s13059-020-1926-6
- Nadukkandy AS et al. (2025). Clinical application of single-cell RNA sequencing in disease and therapy. Clin Transl Med. 15:e70512. https://doi.org/10.1002/ctm2.70512
- Zhu L et al. (2026). Single-cell landscape of immune cells in multiple autoimmune diseases. iScience 29(1): 114515. https://doi.org/10.1016/j.isci.2025.114515
Esta columna se prepara y edita semana con semana, en conjunto con investigadores morelenses convencidos del valor del conocimiento científico para el desarrollo social y económico de Morelos.


